紫外吸收光谱是一种重要的分析手段, 它广泛应用于有机化合物的结构解析和定量分析, 目前已经广泛应用于精细化学品生产、石油化工及环境检测等领域[1], 紫外吸收光谱具有仪器价格便宜及操作简便等优点, 同时紫外吸收光谱的基本原理相对简单、根据紫外吸收光谱可以方便地判别出有机化合物的类型、利用经验规律进行有机化合物的结构解析效果也较好, 特别是利用UV可以确定共扼系统的存在及共扼系统的基本情况。本文总结了紫外吸收光谱在二茂铁及其衍生物结构解析中应用的一般方法。
紫外光测得的电子光谱称紫外光谱, 引起分子中电子能级跃迁的光谱波长范围。10nm~800nm, 紫外光谱波长范围指4nm~400nm之间, 其中波长在4nm~200nm之间称远紫外区, 由于这一区域的紫外光会被O2, 、CO2、N2、H2O等吸收, 因此要除去空气在真空下进行测试, 远紫外区又称真空紫外区。通常所说的紫外光谱是指200nm~400nm波长的近紫外区, 它对有机共轭分子有吸收, 在有机化学中很有价值[1]。
1. 紫外光谱基础知识
1.1 吸收带
紫外吸收光谱是化合物吸收200nm~400nm的紫外线而产生的吸收光谱, 紫外吸收光谱根据有机分子吸收紫外光而产生的不同电子能级跃迁, 将相应的吸收归为不同的吸收带。
1.1.1 R吸收带
n→π跃迁而产生, 例如:-NO2及-CHO等的CH3CHOλmax=291nm, CH2=CHCHOλmax=315nm。特点是吸收波长长, 吸收强度弱 (100左右) 。
1.1.2 K吸收带
共轭双键的例如:CH3CH=CH-CH=CH2, λmax=223nm (ε=22600) 。
1.1.3 E1吸收带:
由苯环的一个共轭双键的电子跃迁引起, 例如苯环的E1吸收带为184nm左右, 吸收强度强 (ε大于10000) 。
1.1.4 E2吸收带
由苯环的两个共轭双键跃迁引起, 例如苯环的E2吸收带为203nm左右, 吸收强度中等 (ε≈7400) 。
1.1.5 B吸收带
由苯环的两个共轭双键跃迁引起, 为一宽峰, 由若干个小峰组成 (称细微结构) , 波长230nm~270nm, 中心在254nm (ε≈204) , 例如:苯乙酮:λmax319nm、ε=50, 为R吸收带, λmax240nm、ε=13000, 为K吸收带, λmax278nm、ε=1100, 为B吸收带[2]。
1.2 红移
由于内部或外部条件的影响使紫外最大吸收波长增加的现象。
1.3 蓝移
由于内部或外部条件的影响使紫外最大吸收波长减小的现象[3]。
2. 紫外吸收光谱的应用
2.1 鉴别一个有机物是否含有共轭体系或芳香结构
例如几个官能团之间是否存在相互共扼, 以及在共扼体系中取代基的位置、种类、数目等, 尤其在确定天然有机物和新化合物的化学结构中, 这是最重要的一环。如果一个未知化合物在近紫外区是透明的 (ε<10) , 则说明不存在共轭体系、芳香结构式n-П*、n-б等易于跃迁的基因。如果有吸收光谱, 则根据图形, 有些可以通过经验计算并在各种可能的结构中推测是哪一种, 有些则可与已发表的紫外光谱图相比较, 观察与哪一类型的化合物相似, 便可推测可能具有的相伺或类似的结构部分[4]。
2.2 推测出有机物的结构。
220nm~250nm (ε<1000) 具有强吸收带的化合物, 可能是含有两个不饱和单位的共轭系 (如共轭二烯或α, β一烯酮等, 如果类似的强吸收峰分别落在2600、300或330nm左右, 则可能含有3, 4或5个不饱和单位的共轭系统。如在200nm~300nm左右有中等强度吸收峰 (εmax=200-1000) 则可能有苯环存在, 如在290nm左右有低强度的吸收峰 (ε=20-100) 可能是醛或酮。
2.3 鉴定化合物的纯度
紫外光谱的灵敏度很高, 容易检验出化合物中所含的微量杂质。由于能吸收紫外光的物质其E很高, 所以一些对近紫外光透明的溶剂或有机物, 果其中的杂质能吸收近紫外光的, 只要 (ε>2000) , 检出的灵敏度可达0.005%如环己烷中常含有杂质苯, 则在255nm处会出现苯的紫外吸收峰。有些高分子化合物对单体纯度要求很高, 如尼龙单体1, 6-己二胺和1, 6-己二酸中若含有微量不饱和或芳香杂质, 可干扰直链高聚物的生成, 从而影响其质量。但这两个单体本身在近紫外区是透明的, 因此用这一方法检验是否存在不必要的物质是很方便和灵敏的。
2.4 判断化合物的构型
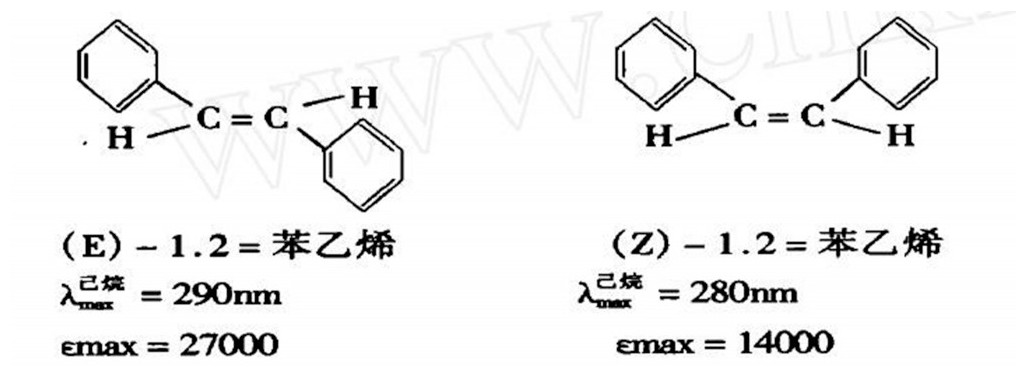
根据不同构型的化合物在近紫外区的吸收不同, 可以判断其构型。如肉桂酸异构体的吸收光谱有很大不同, 反式肉桂酸为平面结构, 双键与处于同一平面的苯环容易发生П-П共轭, 顺式肉桂酸中由于空间位阻, 双键与苯环处于非平面, 不易发生共轭, 反式较顺式εmax位于长波端, εmax高于顺式一倍。
2.5 对平衡体系进行研究
某些有机化合物存在互变异构平衡, 在溶剂极性或不同的条件下, 随着平衡的移动, 其紫外光谱亦发生很大变化, 可利用紫外光谱对这类平衡体系进行研究。如乙酰乙酸乙酯存在酮式和烯醇式两种构体的互变异构平衡, 各自具有特征的紫外光谱。在极性水溶液中, 272nm出现弱吸收带 (ε=16) 。应属酮式异构体的R带, 在非极性溶液如己烷中, 243nm出现强吸收带, 应属烯醇式异构体的K带。显然极性溶液利于酮式异构体的存在, 是由于酮式异构体与质子性极性溶液形成氢键非极性溶剂利于烯醇式异构体的存在, 是由于非极性溶剂中烯醇式易形成分子内氢键。测定不同极性溶剂中异构体比例, 可计算不同溶液中互变异构平衡的平衡常数[5]。
3. 紫外光谱的影响因素
3.1 电子效应对紫外光谱的影响
电子效应包括诱导效应和共轭效应, 前者是由原子或基团的电负性的差异而产生的, 是一种永久效应, 后者是由原子或基团的共平面, 某些化学键或原子轨道发生交盖重叠, 导致电子离域, 电子云密度的分布平均化, 这种现象称为共轭效应。具有电子离域现象实体 (分子、离子游离基等) 称为共轭体系。参与共轭的原子或基团必须共平面, 共平面被破坏, 则共轭体系所呈现的共轭效应随之消失, 即共轭效应不是永久效应。在电子效应中, 对紫外光谱影响最大的是共轭效应, 它直接影响λmax和εmax, 因此, 紫外光谱仅用于含共轭体系的某些不饱和化合物的检测和鉴定[6]。
对共轭多烯烃而言, 每增加一个共轭双键紫外光谱的λmax红移30nm~40nm。
由上例看出, 在π-π共轭体系中, 紫外光谱的λmax (最大吸收峰的峰位) 及εmax (最大吸收峰的峰强) 都是随着共轭链的增长而明显增长 (λmax红移, εmax增强) , 这是因为随着共轭程度的增大, 新组成的π分子轨道与π*分子轨道之间的能级差 (△E) 减小, 即电子跃迁能级差减小, 所需吸收的光子的频率减少, 相应波长增长, 故信号λmax红移。随着△E的减小, 电子跃迁概率明显增大, 故εmax随之增大。
3.2 空间效应对紫外光谱的影响
所谓空间效应是指分子内的原子或基团在三维空间中的位置发生变更或体积有所变化, 导致原子或基团间的作用发生变化, 进而影响物质的性质 (理化性质, 光学性质, 生物性质等) 发生变化, 此种现象, 称为空间效应 (又叫立体效应) 空间效应对紫外光谱的影响[7]。
在上例顺反异构体中, 由于苯基在空间的位置不同, 基团间的作用不同, 共平面的程度不同, 共轭程度不同, 因而导致紫外光谱中的λmax和εmax不同。在 (Z) -1.2=苯乙烯分子内, 二个体积较大的苯基位于烯键的同侧, 苯基间的作用较强, 导致分子中二个苯基和二个H共平面程度减弱, 共轭程度随之减弱, π→π*电子跃迁能级差 (△E) 增大, 故λmax紫移, 即比 (E) -1.2=苯乙烯紫移10nm, 相应的εmax也减小13000, (E) -1.2二苯乙烯中的情况恰好相反, 二个苯环位于双键异侧, 空间距离较远, 团间的作用较弱) , 四个基团 (二个苯基, 二个氢原子) 可以充分地共平面, 共轭程度大, π→π*电子跃迁能级差小, 故λmax=290nm比 (Z) -1.2=苯乙烯长10nm, 由于跃迁能级差小, 电子跃迁概率也相应增 (εmax=2700) , 由上例看出, 空间效应和电子效应是相互联系着的, 利用紫外光谱可以鉴别某些立体异构体的构型[8]。
3.3 溶剂效应对紫外光谱的影响
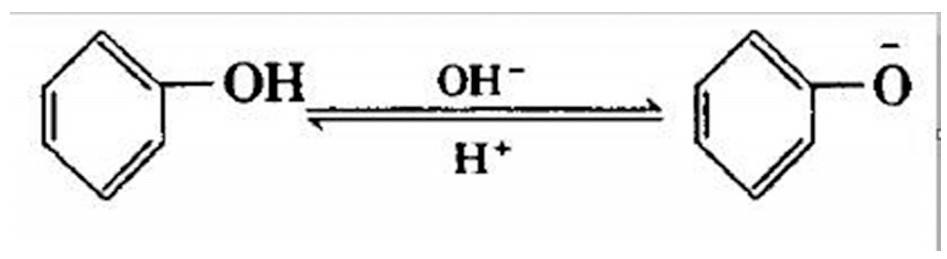
所谓溶剂效应, 是指溶剂的极性或组成不同使反应物 (底物和试剂) 的性质发生一定的变化, 此种现象统称为溶剂效应。在研究紫外光谱时发现, 对π→π*跃迁来说, 溶剂的极性越强, π*中的电子易与溶剂分子结合, 稳定性增强, 能量降低, 导致π→π*, 跃迁能级差 (△E) 减小, λmax红移, 反之亦然。此外, 在测定酸性或碱性物质时, 溶剂的p H值对紫外光谱有很大影响。例如, 苯酚在酸碱溶液中的离解情况不同, 其λmax不同。
据此, 可利用不同PH条件下紫外光谱变化的规律, 确定分子结构中的酸碱基团。
4. 紫外光谱对有机化合物的分析
1, 1′一二乙酰基缩水杨酰腙对二茂铁基苯甲酸乙酯
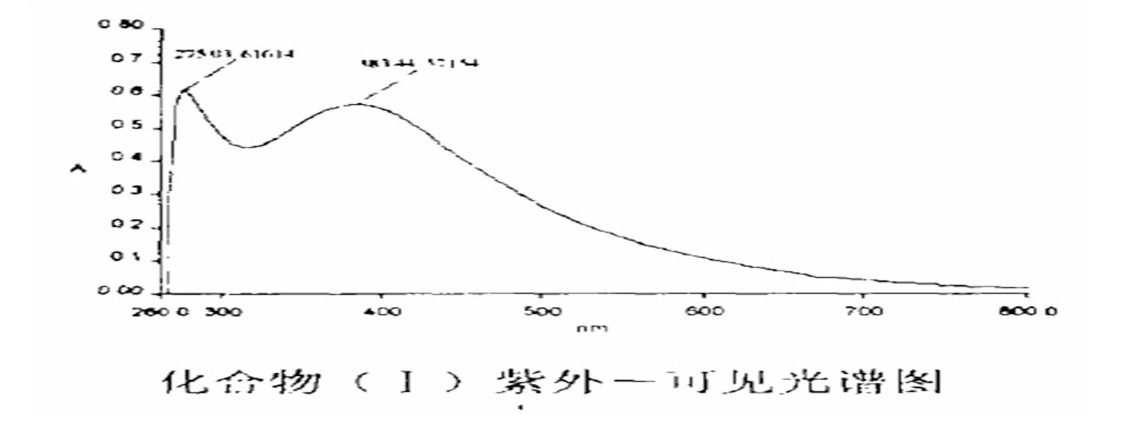
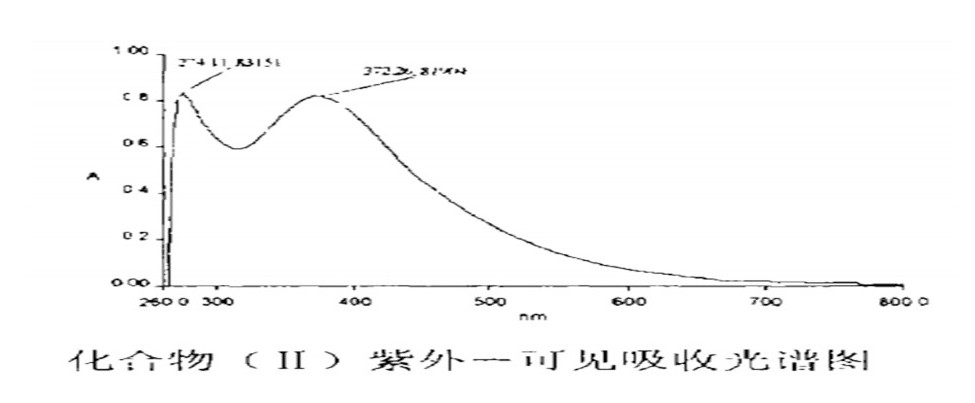
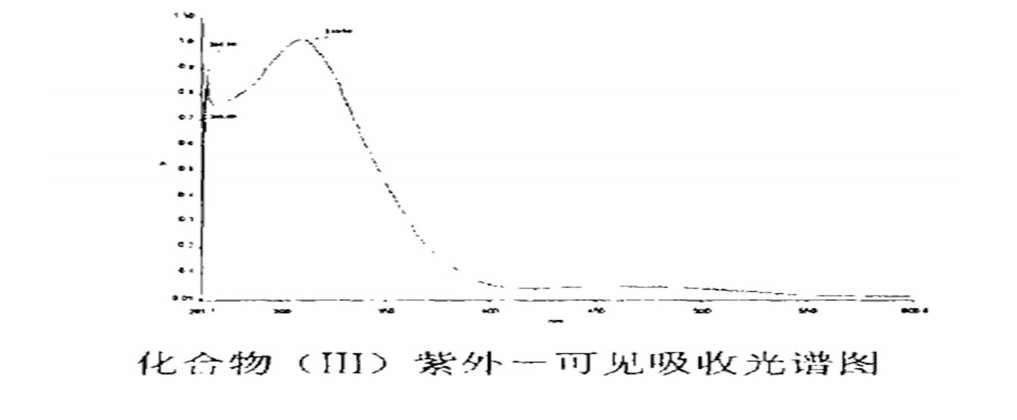

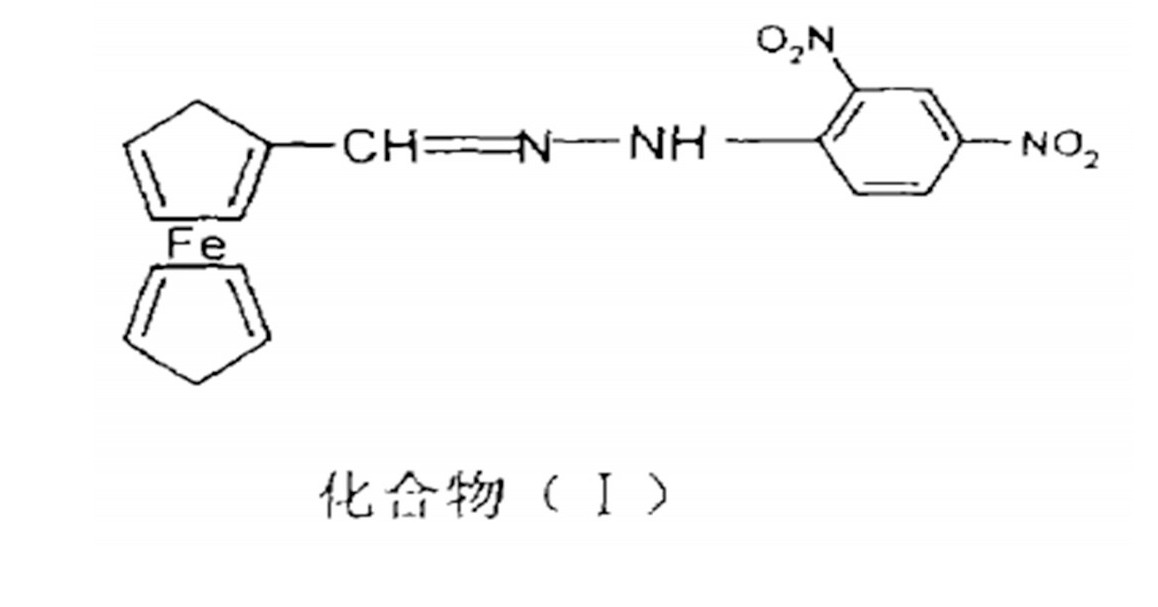
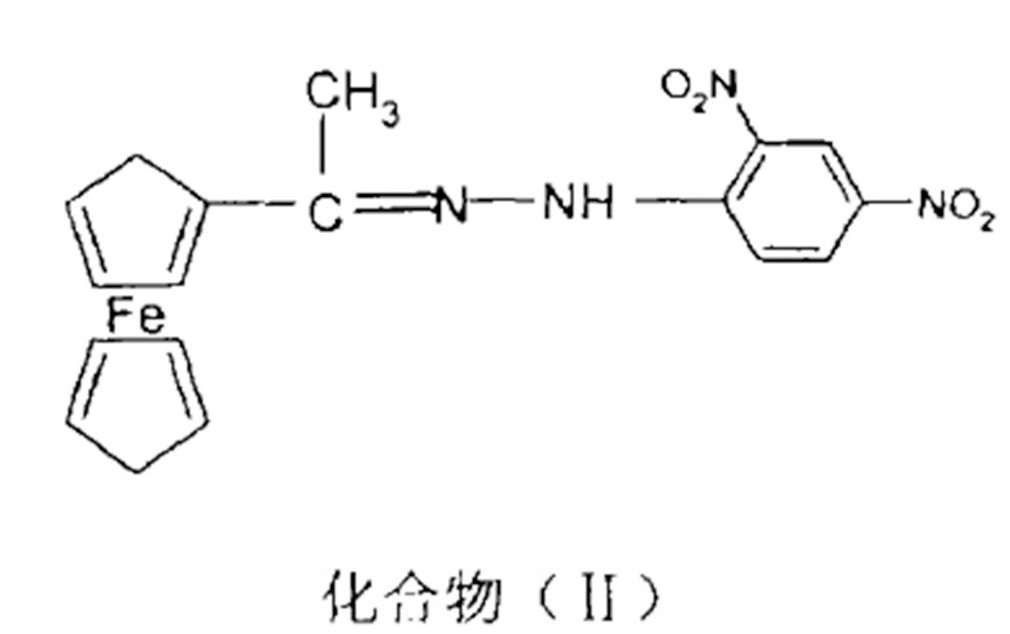
在化合物 (I) 中, 275nm可能是苯胺基部分和亚胺基部分的重叠跃迁, 383nm是C.T吸收带;在化合物 (II) 中274为苯胺基部分跃迁与亚胺基部分跃迁的重叠吸收峰, 372nm为化合物的C.T吸收带;化合物 (III) 中264nm为亚胺基部分和酞胺基部分的重叠跃迁, 310nm为化合物的C.T吸收带;在化合物 (IV) 中, 260nm为苯甲酰基的部分跃迁, 295nm为酯基的部分跃迁, 362nm为化合物的C.T吸收带。在化合物 (I) ~ (III) 中, C.T吸收带波长依次降低, 说明金属与配体之间的电荷转移趋势增强, 也进一步说明茂环上取代基的吸电子能力增强。
由于C.T带的跃迁是禁阻的, 因而化合物 (I) 一 (IV) 都是低强度吸收。化合物 (I) 、 (II) 、 (IV) 的C.T吸收带在370nm附近, 而化合物 (IIl) 落在310nm, 其原因可能是二取代的吸电子基团使二茂铁电荷转移更为显著, 发生蓝移现象。紫外一可见光谱研究表明, 化合物 (I) ~ (IV) 都有电荷转移吸收带 (CT带) , 还存在不同程度的共扼基团吸收峰[9]。
5. 总结
(1) 如果紫外光谱在200nm~400nm无吸收, 则该化合物应无共轭双键系统, 或为饱和有机物。
(2) 如果在UV中270nm~350nm之间给出一个很弱的吸收峰 (εmax=10~100) , 并且在200nm以上无其他吸收。则该化合物含有非键电子的n*p跃迁。相应的结构:C=C—O, C=O等[10]。
(3) 如果在UV中给出许多吸收峰, 某些峰甚至出现在可见光区, 则该化合物存在稠环芳香发色团或长链共轭体系 (4~5个以上C=C) , 但一些含氮化合物及碘仿等除外。
(4) 在UV中, 长波吸收峰的εmax在10000~20000之间时, 表明有A, B不饱和酮或共轭烯烃结构。
(5) 化合物在250nm以上εmax1000~10000有吸收, 而且具有细微结构, 说明芳环的存在。
 发布时间:2025-11-23
发布时间:2025-11-23